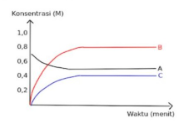
pada temperatur tertentu, terjadi kesetimbangan antara a, b dan c.
data konsentrasi a, b dan c terhadap waktu ditunjukkan pada grafik diatas. reaksi kesetimbangan yang terjadi adalah ….
a. A + B ⇌ C
b. A + C ⇌ 2B
c. A ⇌ 2B + C
d. A ⇌ 4B + 2C
e. 5A ⇌ 8B + 4C
Jawaban yang benar adalah d. A ⇌ 4B + 2C
Kesetimbangan kimia melibatkan reaksi dua arah. Pada awal proses reaksi, terjadi reaksi ke kanan yang menyebabkan zat-zat produk bertambah. Sesaat setelah produk terbentuk terjadi reaksi sebaliknya (reaksi ke kiri) yaitu pembentukan zat-zat reaktan. Jika laju reaksi ke arah produk sama dengan laju reaksi ke arah reaktan, tercapai keadaan setimbang.
Pada saat setimbang konsentrasi reaktan dan produk tidak berubah (tetap). Oleh karena reaksi berlangsung terus-menerus dengan laju reaksi yang sama, kesetimbangan kimia juga disebut kesetimbangan dinamis.
Dari grafik tersebut kita bisa menentukan bahwa zat A merupakan reaktan karena jumlah molnya berkurang, sedangkan zat B dan C merupakan produk karena mula-mula tidak ada lalu terbentuk pada saat reaksi.
Reaksi__A ==> B + C
m_____0,7___0___0
r______0,2__0,8__0,4
s______0,5__0,8__0,4
Pada saat bereaksi dihasilkan perbandingan
A : B : C = 0,2 : 0,8 : 0,4.
A : B : C = 1 : 4 : 2
Dengan menggunakan konsep perbandingan mol = perbandingan koefisien, maka reaksi kesetimbangan yang terjadi A ⇌ 4B + 2C
Dengan demikian, eaksi kesetimbangan yang terjadi adalah A ⇌ 4B + 2C.
Daftar isi
 IlmuanTekno Berita tentang Gadget, Teknologi, Trading, Forex, Saham, Investasi, Bisnis, dan Info Keuangan.
IlmuanTekno Berita tentang Gadget, Teknologi, Trading, Forex, Saham, Investasi, Bisnis, dan Info Keuangan.