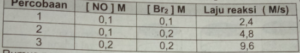
pengamatan laju reaksi :
NO + Br2 –> NOBr2
rumus persamaan laju reaksi yang benar adalah …
a. v = k[NO]2 [Br2]
b. v = k[NO]2 [Br2]2
c. v = k[NO] [Br2]2
d. v = k[NO] [Br2]
e. v = k[Br2]
Jawaban : d. v = k[NO][Br2]
Laju reaksi adalah laju yang diperlukan suatu senyawa untuk bereaksi (Reaktan mengalami pengurangan komposisi, sedangkan produk mengalami pertambahan komposisi). Laju reaksi sebanding dengan konsentrasi reaktan dengan ordenya masing-masing. Misalkan dimiliki reaksi :
A + B => C + D
Maka laju reaksinya dirumuskan dalam
v = k[A]^m[B]^n
Dengan :
k = konstanta laju reaksi
[A] = konsentrasi senyawa A (M)
[B] = konsentrasi senyawa B (M)
m = orde terhadap senyawa A
n = orde terhadap senyawa B
v = laju reaksi (M/s)
Untuk persamaan reaksi NO + Br2 –> NOBr2, didapatkan persamaan laju reaksi sementara sebagai berikut :
v = k[NO]^m[Br2]^n
Bandingkan data kedua dan ketiga untuk memperoleh nilai m sebagai berikut :
4,8 M/s = k(0,1 M)^m(0,2 M)^n
9,6 M/s = k(0,2 M)^m(0,2M)^n
___________________________ :
1/2 = (1/2)^m
m = 1
Bandingkan data pertama dan kedua untuk memperleh nilai n sebagai berikut :
2,4 M/s = k(0,1 M)^m(0,1 M)^n
4,8 M/s = k(0,1 M)^m(0,2M)^n
___________________________ :
1/2 = (1/2)^n
n = 1
Dengan demikian, persamaan laju reaksinya adalah v = k[NO][Br2]
 IlmuanTekno Berita tentang Gadget, Teknologi, Trading, Forex, Saham, Investasi, Bisnis, dan Info Keuangan.
IlmuanTekno Berita tentang Gadget, Teknologi, Trading, Forex, Saham, Investasi, Bisnis, dan Info Keuangan.