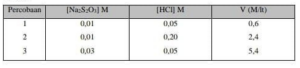
Pada percobaan reaksi antara larutan Na2S2O3 dengan larutan HCl diperoleh data sebagai berikut:
Tentukan Orde reaksi HCl
orde reaksi HCl adalah 1.
Ayo simak pembahasan berikut agar lebih paham.
Laju reaksi adalah laju bertambahnya produk tiap satuan waktu atau laju berkurangnya reaktan tiap satuan waktu. Percobaan laju reaksi dapat digunakan untuk menentukan orde reaksi dan persamaan laju reaksi.
Untuk menentukan orde reaksi HCl, diperlukan 2 data laju reaksi untuk dibandingkan. Data yang dipilih adalah data dengan konsentrasi HCl berbeda dan konsentrasi Na2S2O3 sama.
Misalkan orde Na2S2O3 = a dan orde HCl = b
v1/v2 = k [Na2S2O3]^a [HCl]^b / k [Na2S2O3]^a [HCl]^b
0,6/2,4 = (0,01)^a (0,05)^b / (0,01)^a (0,20)^b
1/4 = (0,05)^b / (0,20)^b
1/4 = (1/4)^b
b = 1
Jadi, orde reaksi HCl adalah 1.
Daftar isi
 IlmuanTekno Berita tentang Gadget, Teknologi, Trading, Forex, Saham, Investasi, Bisnis, dan Info Keuangan.
IlmuanTekno Berita tentang Gadget, Teknologi, Trading, Forex, Saham, Investasi, Bisnis, dan Info Keuangan.